Vodný experiment
Dokáže sa voda zmeniť na zlato?
Možná existencia kovovej vody V súčasnosti je známe, že nefiltrovaná voda môže viesť elektrinu. Príčinou je, že obsahuje vysoké množstvo soli, preto môžu záporne nabité elektróny ľahko prúdiť medzi jej molekulami. Vyčistená voda však obsahuje iba molekuly vody, ktorých najvzdialenejšie elektróny zostávajú viazané na ich určené atómy. To je dôvod, prečo nemôžu voľne prúdiť čistou vodou…. Prečítať celé
Možná existencia kovovej vody
V súčasnosti je známe, že nefiltrovaná voda môže viesť elektrinu. Príčinou je, že obsahuje vysoké množstvo soli, preto môžu záporne nabité elektróny ľahko prúdiť medzi jej molekulami. Vyčistená voda však obsahuje iba molekuly vody, ktorých najvzdialenejšie elektróny zostávajú viazané na ich určené atómy. To je dôvod, prečo nemôžu voľne prúdiť čistou vodou.
Čo sa týka teoretickej roviny, ak by sa na čistú vodu aplikoval dostatočný tlak, molekuly vody by sa stlačili dohromady a najvzdialenejšie elektróny by sa prekryli. To by im umožnilo voľne prúdiť medzi každou molekulou a technicky by premenilo vodu na kov. Na túto metódu by ale bol potrebný obrovský tlak, ktorý na Zemi nie je možný. Preto sa vedci domnievajú, že kov sformovaný z vody by sa mohol nachádzať v jadrách obrovských planét ako Jupiter, Neptún a Urán.
Nový experiment ukazuje zaujímavé výsledky
Praktický experiment ukázal nielen prevratný výsledok, ale pre vedcov znamenal aj odklonenie sa od menej zábavných činností. Predpoklad na vykonanie analýzy tkvel v spôsobe, akým by sa voda mohla stať vodičom elektriny. Ide o „požičiavanie“ elektrónov z alkalických kovov, v tomto prípade sodíka a draslíka. Tieto reaktívne prvky majú tendenciu darovať svoj najvzdialenejší elektrón.
„Vôbec sme si neboli istí že to nájdeme. Bolo to úžasné, ako keď objavíte nový prvok,“ hovorí Pavel Jungwirth, fyzikálny chemik z Českej akadémie vied v Prahe. Predtým viedol podobný pokus so svojím kolegom, Philipom Masonom (ktorý vedecké videá zverejňuje na Youtube), kedy experiment vykonávali na amoniaku. Skutočnosť, že amoniak sa v takýchto podmienkach môže lesknúť, vedel už britský chemik Humphry Davy na začiatku 19. storočia.
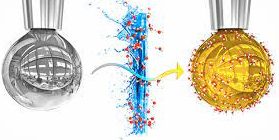
Aj keď ide o prelomový úspech experimentu, slúži hlavne k spopularizovaniu vedy. zdroj: nanowerk.com
Predtým, než skupina začala so skúmaním, čelila výzve. Alkalické kovy zvyknú pri zmiešaní vodou reagovať výbušne. Riešením bolo navrhnúť zostavu, ktorá by dramaticky spomalila reakciu, aby nedošlo k explózií. Experimenty na kruhovom urýchľovači častíc (synchrotrón) v Berlíne potvrdili, že zlatá vrstva preukázala znaky očakávané od kovovej vody. Kľúčom k zabráneniu výbuchu bolo nájsť časové okno, v ktorom bol rozptyl elektrónov rýchlejší ako reakcia medzi vodou a kovmi.
Výskumníci naplnili injekčnú striekačku sodíkom a draslíkom. Takáto zmes je pri izbovej teplote tekutá. Následne ju umiestnili do vákuovej komory. Potom použili striekačku na vytvorenie kvapiek kovovej zmesi a vystavili ich malým množstvám vodnej pary. Voda sa na každej kvapke zrazila a vytvorila vrstvu s hrúbkou jednej desatiny mikrometra. Elektróny z kvapôčky sa rýchlo rozptýlili do vody – spolu s kladnými kovovými iónmi – a v priebehu niekoľkých sekúnd sa vodná vrstva zmenila na zlatú.
Keď voda porušuje zákony fyziky
Aj keď si môžeme myslieť, že voda nás svojimi vlastnosťami nemôže prekvapiť, nájdu sa výnimky, ktoré potvrdzujú pravidlo. Dokonca niekoľko pravidiel. Keď kvapka vody dopadne na povrch, ktorý je oveľa teplejší, než je jej bod varu, môže sa pohybovať po povrchu dlhšie, než by ste čakali. Tento jav má dokonca oficiálny názov, a to Leidenfrostov efekt. Vyskytuje sa, keď sa spodná vrstva kvapky vyparí a molekuly plynnej vody v tejto vrstve nemajú kam uniknúť. Ich prítomnosť teda izoluje zvyšok kvapky a bráni jej dotknúť sa horúceho povrchu pod ňou. Kvapka tak prežije niekoľko sekúnd bez toho, aby sa vyparila.
Známy je fakt, že tenučká vrstva tekutiny na povrchu pevného ľadu spôsobuje jeho šmykľavosť. Teoretici špekulovali o dôvode kĺzania. Môže ním byť kontakt topánky s ľadom, vďaka ktorému sa povrch roztopí. Iní sú presvedčení o existencii vrstvy tekutiny je tu ešte predtým, než na ľad stúpime. Podľa nich je nejakým spôsobom generovaná vlastným pohybom povrchových molekúl.
Keď je medzi vodou a vonkajším vzduchom obrovský teplotný rozdiel, nastáva prekvapivý efekt. Voda sa premení na sneh a vyparí sa. V podstate ide o veľkú hustotu extrémne studeného vzduchu a jeho molekuly sú rozmiestnené tak blízko, že neostáva veľa miesta na prenášanie vodnej pary. Na druhej strane vriaca voda veľmi ľahko uvoľňuje paru. Keď sa vyvrhne do vzduchu, rozpadne sa na kvapôčky, ktoré majú ešte väčšiu plochu, z ktorej môžu vystupovať pary. To predstavuje problém. Pary je viac, než dokáže vzduch zadržať, takže sa „vyzráža“ priľnutím k mikroskopickým časticiam vo vzduchu (sodík alebo vápnik) a tvorí kryštály – snehové vločky.
Zdroje: www.livescience.com, www.nature.com
Titulná fotografia: nature.com











